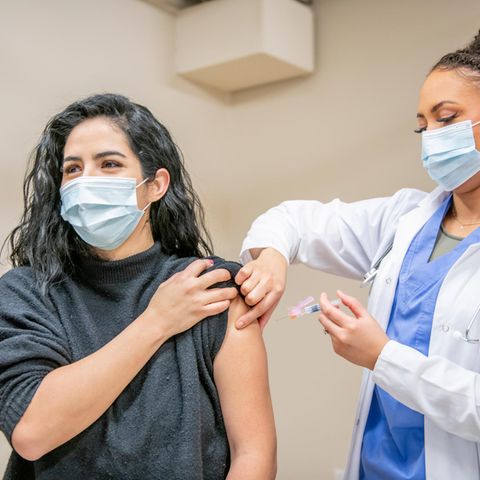
Die Ständige Impfkommission (Stiko) hat sich für die Corona-Impfung mit dem Vakzin des Herstellers Novavax für Menschen ab 18 ausgesprochen. Zudem befürwortet sie eine zweite Auffrischimpfung für gesundheitlich besonders gefährdete und exponierte Gruppen. Das teilte das Expertengremium am Donnerstag zu zwei Beschlussentwürfen mit. Der Novavax-Impfstoff solle neben den bisherigen Covid-19-Impfstoffen zur Grundimmunisierung mit zwei Dosen im Abstand von mindestens drei Wochen bei volljährigen Menschen eingesetzt werden. Für Schwangere und Stillende werde der Impfstoff aktuell jedoch nicht empfohlen.
Es handelt sich noch nicht um finale Stiko-Empfehlungen, es läuft nun noch ein Abstimmungsverfahren mit Fachgesellschaften und Ländern. Änderungen seien noch möglich.
Zuvor hatte das Gremium angekündigt, dass eine derartige Empfehlung geplant sei. "Die jüngsten Daten aus Israel legen nahe, dass eine vierte Dosis eine gewisse Verbesserung beim Schutz vor Infektion und eine deutlichere Verbesserung beim Schutz vor schwerer Erkrankung bewirkt", sagte der Stiko-Vorsitzende Thomas Mertens den Zeitungen der Funke-Mediengruppe.
Infektionsschutz schwindet wieder
Für Menschen ab 70 Jahren, Menschen in Pflegeeinrichtungen, Menschen mit Immunschwäche ab fünf Jahren sowie Beschäftigte in medizinischen Einrichtungen und Pflegeeinrichtungen soll es aus Sicht der Stiko zudem eine zweite Auffrischimpfung mit einem mRNA-Impfstoff nach abgeschlossener Grundimmunisierung und der ersten Auffrischimpfung geben. Bei gesundheitlich gefährdeten Menschen solle diese frühestens drei Monate nach der ersten Auffrischimpfung erfolgen, Personal in medizinischen und pflegerischen Einrichtungen solle den zweiten Booster frühestens nach sechs Monaten erhalten.
Zur Begründung teilte das Gremium mit, dass aktuelle Daten einen schwindenden Infektionsschutz nach der ersten Auffrischimpfung gegen die Omikron-Variante binnen weniger Monate zeigten. Das sei besonders für Menschen ab 70 und Menschen mit Immunschwäche, die am gefährdetsten für einen schweren Verlauf bei einer Infektion seien, ein Risiko. Der zweite Booster solle nun den Schutz verbessern.
Für Menschen, die nach der ersten Auffrischimpfung eine Corona-Infektion durchgemacht hätten, werde aber kein weiterer Booster empfohlen, hieß es. Die Stiko geht beim zweiten Booster von einer ähnlichen Verträglichkeit aus wie beim ersten. Das Gremium erklärte aber auch, "dass die Datenlage zur Effektivität und zur Sicherheit einer zweiten Auffrischimpfung noch limitiert ist".
Israel impft alle Risikogruppen ab 18 zum vierten Mal
Daten, die eine allgemeine Empfehlung zur vierten Impfung mit den bisherigen Impfstoffen nahelegen, lägen dagegen bisher nicht vor, sagte Dahmen. "Die allermeisten Menschen haben bisher in Deutschland ihre Booster-Impfung im Dezember oder Januar bekommen. Ihr Immunschutz vor schwerer Erkrankung ist aktuell sehr gut."
Israel hatte jüngst den Kreis der Berechtigten für eine vierte Corona-Impfdosis ausgeweitet. In der neuen Phase der Booster-Kampagne können auch alle immungeschwächten Menschen ab 18 Jahren eine vierte Impfstoffdosis erhalten. Dasselbe gilt für Menschen, die durch ihren Beruf einem hohen Ansteckungsrisiko ausgesetzt sind. Bislang war die vierte Impfstoffdosis nur für ältere und besonders gefährdete Bevölkerungsgruppen verfügbar.
Erster Proteinimpfstoff für alle Erwachsenen ab 18 Jahren
Zudem empfiehlt die Stiko den Einsatz des Corona-Impfstoffs von Novavax für Menschen ab 18. Der Proteinimpfstoff solle zur Grundimmunisierung mit zwei Dosen im Abstand von mindestens drei Wochen eingesetzt werden, teilte das Expertengremium am Donnerstag mit. Ein entsprechender Beschlussentwurf sei zur Abstimmung an Fachkreise und Bundesländer gegangen, daher seien Änderungen noch möglich.
Bei dem Präparat Nuvaxovid des US-Herstellers Novavax, das seit Ende Dezember in der EU zugelassen ist, handelt es sich – anders als bei den anderen zugelassenen Vakzinen – um einen Proteinimpfstoff mit einem Wirkverstärker. "In den Zulassungsstudien zeigte der Impfstoff eine mit den mRNA-Impfstoffen vergleichbare Wirksamkeit", erklärte die Stiko. Zur klinischen Wirksamkeit gegen die Omikron-Variante könnten aber noch keine Aussagen getroffen werden.
Das Novavax-Vakzin, das in Deutschland ab dem 21. Februar verfügbar sein soll, könne zu ähnlich ausgeprägten Impfreaktionen führen wie die anderen zugelassenen Vakzine gegen das Coronavirus. "Die Zulassungsstudien ergaben keine Sicherheitsbedenken hinsichtlich schwerer unerwünschter Wirkungen nach Impfung", schreibt die Stiko. Allerdings sei die Datenlage zu Nuvaxovid noch begrenzt.