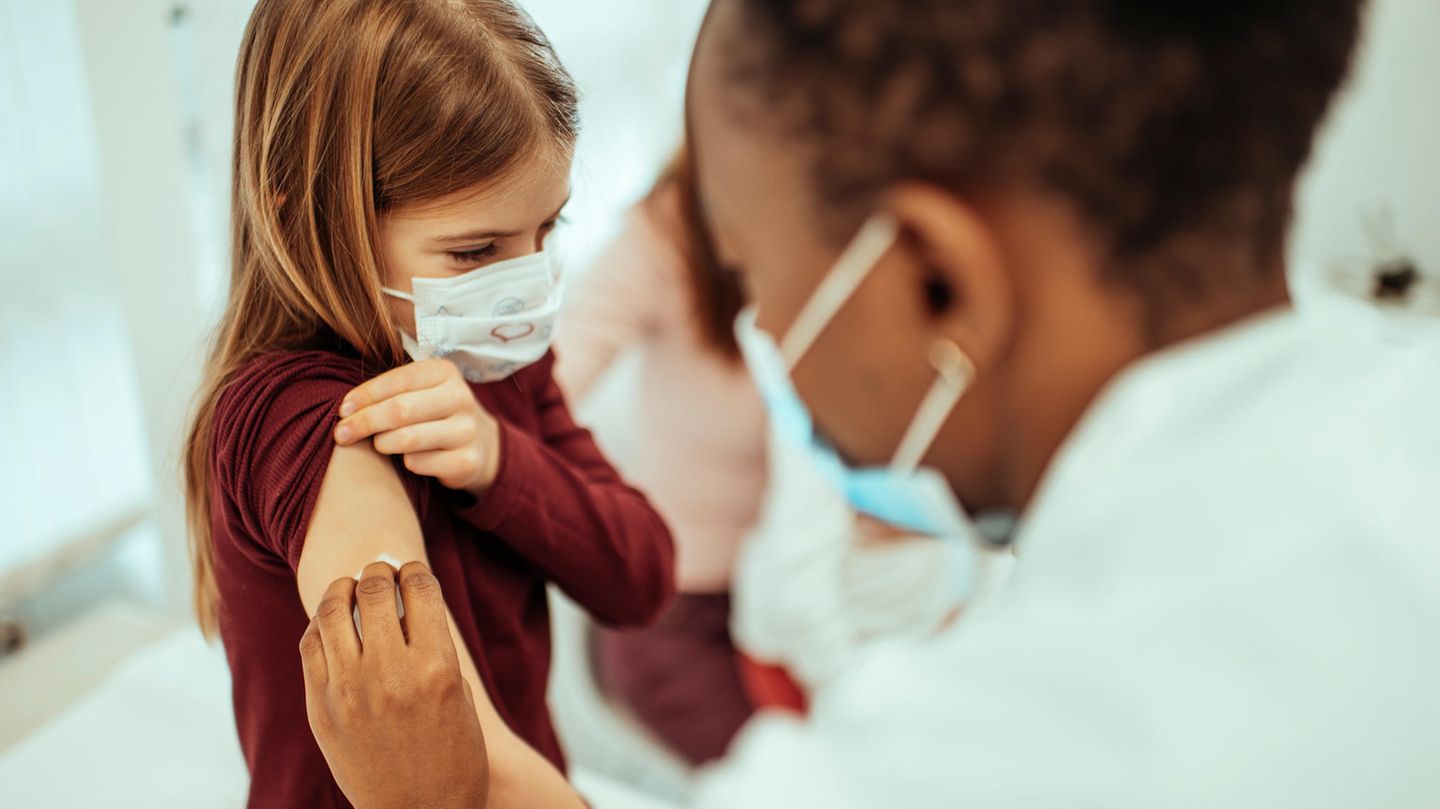
In den USA hat das Warten für viele Familien ein Ende: Seit gestern empfiehlt die Gesundheitsbehörde CDC den Kinder-Corona-Impfstoff der Hersteller Biontech/Pfizer für die Altersgruppe der Fünf- bis Elfjährigen. Bereits in der vergangenen Woche hatte die US-Arzneimittelbehörde FDA dem Impfstoff eine Notfallzulassung erteilt. Anlaufen soll die Impfkampagne bereits in dieser, spätestens aber in der kommenden Woche.
Auf der Zulassung ruht ein Schlaglicht, da in den USA und der Europäischen Union bislang kein Corona-Impfstoff für diese Altersgruppe zugelassen war. Kinder und Jugendliche ab zwölf Jahren können sich dagegen seit einigen Monaten mit Impfungen vor Covid-19 schützen. Für sie ist der Impfstoff des deutschen Herstellers Biontech und seines US-Partners Pfizer bereits zugelassen. Ebenfalls infrage kommt ein weiteres mRNA-Vakzin – das des US-Unternehmens Moderna.
Kinder erkranken nur sehr selten schwer an Covid-19. Allerdings gibt es Ausnahmen: In den USA haben sich bislang 1,9 Millionen Kinder zwischen fünf und elf Jahren mit dem Virus angesteckt. Mehr als 8300 von ihnen mussten in einer Klinik behandelt werden, mehr als 100 Kinder starben. Bekannt ist auch, dass das Coronavirus bei Kindern zu einem sogenannten Multisystemischen Entzündungssyndrom führen kann – einer ernsten Spätfolge einer Infektion. Die USA listen mehr als 2300 Fälle. Auch Long-Covid-Beschwerden bei Kindern wurden bereits beschrieben. Mit der Zulassung eines Impfstoffs für diese Altersgruppe ist die berechtige Hoffnung verbunden, dass solche Fälle in Zukunft verhindert werden können.
Welche Daten zu dem Impfstoff liegen bislang vor? Und wann ist mit einer Zulassung in der Europäischen Union (EU) zu rechnen? Ein Überblick über die wichtigsten Infos.
Wie setzt sich der Impfstoff zusammen?
Der Impfstoff für jüngere Kinder basiert wie der Erwachsenen-Impfstoff von Biontech/Pfizer auf der bekannten mRNA-Technologie. Impfstoffe dieser Art enthalten den Bauplan für ein Protein des Coronavirus: das Spike-Protein, mit dem Sars-CoV-2 an menschliche Zellen andockt.
Für den vollen Impfschutz sind wie beim Erwachsenen-Impfstoff zwei Dosen im Abstand von drei Wochen nötig. Die Dosierung ist geringer. Sie liegt bei jeweils zehn Mikrogramm mRNA und beträgt damit ein Drittel der Menge des Erwachsenen-Impfstoffs.
Wie gut wirkt der Impfstoff? Was weiß man über mögliche Nebenwirkungen?
Die Hersteller Biontech/Pfizer legten kürzlich Daten vor, wonach der Kinder-Impfstoff in der Altersgruppe von fünf bis elf Jahren eine Wirksamkeit von 90,7 Prozent zeigte. Das entspricht einer sehr hohen Schutzwirkung. An der dazugehörigen Studie nahmen rund 4500 Kinder teil.
Sicherheitsbedenken gibt es auf Grundlage dieser Studie nicht. Allerdings ist die Zahl der Probanden bislang noch recht gering. Die Wahrscheinlichkeit, mit der womöglich seltene Nebenwirkungen auftreten, lässt sich daher nach Ansicht einiger Experten noch nicht zuverlässig abschätzen. Nach der zweiten Dosis bisher zugelassener mRNA-Impfstoffe wurde bei jungen Männern eine gewisse Neigung zu Herzmuskel- und Herzbeutelentzündungen beobachtet. Die Entzündung ist zumeist gut zu behandeln und tritt auch nach Covid-19-Erkrankungen auf.
Die Gesundheitsbehörden in den USA werden deshalb in den kommenden Wochen besonders aufmerksam sein, ob diese seltene Nebenwirkung auch nach Impfungen mit dem Kinder-Vakzin auftritt. Experten gehen aber davon aus, dass – sollte es zu der Nebenwirkung kommen – diese selten sein wird.
Nach der Zulassung wird die Sicherheit von Impfstoffen fortlaufend überwacht. In Deutschland ist dafür das Paul-Ehrlich-Institut (PEI) zuständig.
Wann können Kinder in Deutschland gegen das Coronavirus geimpft werden?
Die Unternehmen Biontech/Pfizer haben bereits eine EU-weite-Zulassung des Impfstoffs für Kinder zwischen fünf und elf Jahren beantragt. Als wahrscheinlich gilt, dass die zuständige Stelle – die Europäische Arzneimittel-Agentur (EMA) – bis Weihnachten über den Antrag entscheidet. Gibt sie grünes Licht, muss die Europäische Kommission der Zulassung formal zustimmen. Im Anschluss kann mit der Auslieferung der Vakzine und den Impfungen begonnen werden.
Fraglich ist allerdings, ob die Ständige Impfkommission (Stiko) zu diesem Zeitpunkt bereits eine Empfehlung für die Altersgruppe ausgesprochen haben wird. Das wissenschaftliche Gremium ist bekannt dafür, zurückhaltend zu agieren, sollten belastbare Daten fehlen. Bereits bei der Impfung für Kinder zwischen 12 und 17 Jahren hatte die Stiko das Vakzin zunächst für Patienten mit bestimmten Vorerkrankungen empfohlen. Erst einige Wochen später, als weitere Daten vorlagen, folgte die allgemeine Empfehlung. Zwar ist eine Stiko-Empfehlung für eine Impfung nicht zwingend nötig. In der Praxis orientieren sich aber viele Medizinerinnen und Mediziner an ihr.
Stiko-Chef Thomas Mertens hatte sich bislang zurückhaltend zu einer möglichen Empfehlung für Kinder zwischen fünf und elf Jahren geäußert und auf geringe Probandenzahlen in Zulassungsstudien verwiesen. "Solche Zulassungsstudien sind nicht dazu ausgelegt, allein aufgrund der Anzahl der Probanden, dass man damit sämtliche Risiken ausschließen kann", sagte Mertens im Gespräch mit dem "SWR". Da Kinder nur selten schwer an Covid-19 erkrankten, müsse man sehr sicher sein, dass der Impfstoff "auch sehr sicher" sei.
Wann könnte ein Impfstoff für jüngere Kinder unter fünf Jahren zur Verfügung stehen?
Die Hersteller Biontech/Pfizer erproben einen Impfstoff für Kinder unter fünf Jahren bereits in klinischen Studien. Das Vakzin ist noch einmal etwas niedriger dosiert und enthält drei Mikrogramm mRNA. Erste Ergebnisse dieser Untersuchungen könnten nach Herstellerangaben schon bald veröffentlicht werden. Zu einer Zulassung für diese Altersgruppe kommt es allerdings nur dann, wenn die zuständigen Gesundheitsbehörden zu dem Schluss kommen, dass der Nutzen des Impfstoffs mögliche Risiken überwiegt.